В первой половине этого года Национальная групповая стандартная информационная платформа анонсировала Технические рекомендации по стратегиям контроля загрязнения (CCS) при производстве стерильных лекарств (T/CPAPE 01-2024), организованные Китайской ассоциацией разработчиков фармацевтического оборудования. Проект руководства был опубликован 7 сентября 2023 г. и по результатам опроса общественного мнения. Оно официально вступило в силу 1 июня 2024 года. Хотя это руководство не является обязательным, оно предоставляет технические ссылки для фармацевтических производственных и научно-исследовательских компаний, проектных подразделений заводов, производителей оборудования и т. д. и играет важную направляющую роль в улучшение контроля загрязнения в процессе фармацевтического производства.
Появление концепции стратегии контроля загрязнения (CCS) не случайно, а неизбежный выбор для поколений медицинских работников в их стремлении к качеству лекарств...
01
Откуда взялась стратегия контроля загрязнения (CCS)?

Откуда взялась стратегия контроля загрязнения (CCS)?
В декабре 2017 года, когда ЕС опубликовал пересмотренный проект Приложения 1 GMP «Производство стерильных лекарственных средств» («Приложение 1 GMP ЕС»), впервые появилась и официально была принята концепция стратегии контроля контаминации (CCS). подтверждено выпуском «Приложения 1 EU GMP» 22 августа 2022 года. В то же время в поле зрения общественности появилась концепция выпуска параметров. По мере того, как условия реализации продолжают развиваться, контроль процесса производства стерильных лекарств будет переходить от обнаружения к контролю процесса и выпуску параметров.
02
Что такое Стратегия контроля загрязнения (CCS)?
Приложение 1 к GMP ЕС четко определяет стратегию контроля загрязнения (CCS). [2] :

Соответствующие ведомства определяют сферу применения стратегии контроля загрязнения (CCS) следующим образом: [3][4][5] :

03
Почему вас должна волновать стратегия контроля загрязнения (CCS)?
Суть стратегии контроля загрязнения (CCS) заключается в контроле возможных рисков загрязнения во всех аспектах процесса производства лекарственных средств, а также в максимально возможном устранении/снижении/предотвращении рисков загрязнения с помощью научных и систематических мер, чтобы гарантировать, что предприятия может производить высококачественную, безопасную и надежную продукцию. В случае загрязнения результатом являются не только материальные отходы, но и детальное исследование и устранение источника загрязнения, что требует много времени и труда, а также приводит к большим потерям; в серьезных случаях контролирующие органы будут расследовать и наказывать, а то и отзывать товар с рынка, что еще более невыносимо для предприятия.
Типичные этапы разработки и поддержания стратегии контроля загрязнения следующие:
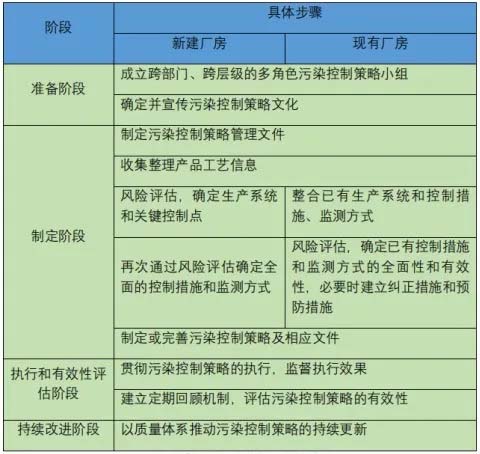
Пример шагов по разработке и поддержанию стратегии контроля загрязнения
Исходя из этого, нетрудно увидеть, что Стратегия контроля загрязнения (CCS) является неизбежным требованием для адаптации к развитию отрасли за пределами Китая. Если соответствующие фармацевтические компании хотят поддерживать соблюдение требований и конкурентоспособность, они должны осознавать, что разработка и поддержание Стратегии контроля загрязнения (CCS) представляет собой динамичный и непрерывный процесс. Если они хотят идти в ногу с международными стандартами, им необходимо включить Стратегию контроля загрязнения (CCS) в собственную систему качества компании, вести соответствующие записи, выдавать соответствующие документы, а также регулярно их обобщать и обновлять.
04
Элементы управления Стратегии контроля загрязнения (CCS)
Заводские мощности
Заводские мощности являются необходимой гарантией качества производства лекарственных средств. Фармацевтическим производителям необходимо организовать профессиональный и технический персонал для планирования и проектирование заводских помещений в соответствии с требованиями различных лекарственных форм лекарственных средств и провести соответствующую проверку, чтобы подтвердить, что их эффективность может удовлетворить ожидаемые потребности. В жизненном цикле заводских объектов одного хорошего проектирования недостаточно. Его использование, обслуживание, ремонт и ежедневный мониторинг также являются незаменимыми звеньями. В то же время заводские помещения необходимо регулярно проверять, чтобы гарантировать, что они могут продолжать эффективно контролировать загрязнение. Формулирование стратегии контроля загрязнения неотделимо от общего рассмотрения всего жизненного цикла заводских объектов.
На примере чистых помещений выбор декоративных материалов напрямую связан с чистотой, безопасностью, долговечностью, эксплуатационными расходами и т. д. Учитывая широкое распространение дезинфекция перекисью водорода (VHP) в чистых помещениях более высокие требования ставятся на коррозионную стойкость перегородки для чистых помещений .
Являясь поставщиком решений по сборке отделочных материалов для чистых помещений и лабораторий, компания Pharma United запустила Панель Asepticlean® Anti-VHP в ответ на этот спрос. После тщательного внутреннего тестирования компании Pharma United и проверки на местах у клиентов этот продукт продемонстрировал значительные преимущества:
- Толщина поверхностного покрытия Фарма Юнайтед Панель Asepticlean® Anti-VHP имеет высоту ≥150 мкм, что намного выше, чем у обычной цветной стальной пластины с предвальцовым покрытием (PPGI), демонстрируя превосходную стойкость к перекиси водорода. Более того, по сравнению с фторуглеродным покрытием предварительного валика (PVDF) и полиэфирным покрытием (PE), Pharma United Asepticlean® Анти-VHP Панель работает лучше по производительности.
- По сравнению с нержавеющей сталью SS304, Панель Asepticlean® Anti-VHP не только позволяет избежать зрительного утомления, но и благодаря простоте ухода также значительно снижает затраты на техническое обслуживание. Он также более доступен по цене, предоставляя пользователям экономически эффективный выбор.
оборудование
Управление оборудованием включает в себя все виды деятельности на всех этапах жизненного цикла оборудования. Эффективная система управления оборудованием может в максимальной степени предотвратить и контролировать потенциальное загрязнение в процессе фармацевтического производства. Проектирование, использование, техническое обслуживание и ремонт оборудования, регулярные проверки и т. д. — все это ключевые моменты стратегии контроля загрязнения. Недостаточный контроль какого-либо фактора или отсутствие связи между факторами может привести к дефектам всей Стратегии контроля загрязнения.
В то же время, хотя экологический мониторинг является эффективным способом отражения уровня загрязнения окружающей среды, вариативность самого метода его мониторинга сравнительно высока. Предприятиям необходимо осознавать, что уровень обеспечения стерильности не зависит от мониторинга окружающей среды и обнаружения симуляции асептического процесса. Данные экологического мониторинга в большей степени касаются выявления изменений в экологическом контроле, а не предоставления количественной информации об уровнях микробов и частиц в окружающей среде.
В целом, с тех пор как Национальное управление по производству медицинской продукции (NMPA) постепенно присоединилось к ICH и стало формальным заявителем на PIC/S, фармацевтические законы и правила Китая стали более согласованными с международными стандартами, что привело к совершенствованию китайских стандартов проверки GMP. координация стандартов инспекции и укрепление регулирующих органов. Независимо от того, производят ли китайские фармацевтические компании и продают их на местном уровне или экспортируют за границу, создание надежной системы стратегии контроля загрязнения (CCS) является необходимой мерой, позволяющей справиться с иностранным надзором и улучшить качество корпоративной продукции.































